(Page créée avec « {{Tuto Details |Main_Picture=Doigts_-_saucisses_IMG_20200407_143014567.jpg |Licences=Attribution (CC-BY) |Description=Sais-tu ce qu'est une illusion d'optique ? En voici u... ») |
|||
| Ligne 32 : | Ligne 32 : | ||
Il faut bien regarder au delà de nos index. | Il faut bien regarder au delà de nos index. | ||
| + | |Explanations=Comme le regard est fixé sur un point à l'horizon, lorsqu'un objet passe entre le regard et le point , il est déformé car l'oeil l'interprête mal. | ||
| + | |Deepen=L'illusion d'optique résulte d'une mauvaise interpretation du système visuel des informations qui lui parviennent. Le système visuel ne fonctionne pas comme un instrument de mesure, mais comme un moyen d'interagir efficacement avec l'environnement. | ||
| + | |||
| + | Dans l'expérience ordinaire, en cas de doute, un changement de point de vue donne une vision plus exacte de la réalité. Dans les illusions visuelles, cette possibilité est bloquée, entraînant une image faussée de la réalité, y compris faisant voir un objet inexistant, ou rendant « aveugle » à un objet pourtant présent. | ||
| + | |||
| + | |||
| + | https://fr.wikipedia.org/wiki/Illusion_d%27optique | ||
| + | |Applications=On peut observer dans la rue des trompe-l'oeil qui créent l'illusion d'une profondeur sur une surface plane vue depuis un certain point. La peinture et le théâtre utilisent également cette technique pour donner des effets de profondeur et de volume. | ||
| + | |||
| + | Les illusionnistes et magiciens en font, aidés par des techniques de persuasion, une bonne part de leurs spectacles. | ||
| + | |Objectives=Le but de cette expérience est d'introduire la notion d'illusion d'optique en montrant que l'on peut modifier notre perception des objets. | ||
| + | |Notes=[https://fr.wikipedia.org/wiki/Illusion_d%27optique Illusion d'optique sur Wikipedia] | ||
}} | }} | ||
{{Tuto Status | {{Tuto Status | ||
|Complete=Draft | |Complete=Draft | ||
}} | }} | ||
Version du 7 avril 2020 à 15:11
Introduction
Étape 2 - Placement
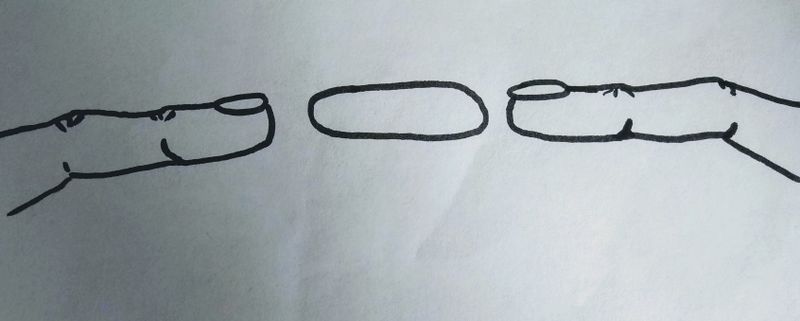
Il suffit simplement de placer tes deux index l'un en face de l'autre à environ 15 cm de tes yeux.
Que vois-tu ?
Comment ça marche ?
Observations : que voit-on ?
On voit qu'il y a une "saucisse" entre nos deux index.
Mise en garde : qu'est-ce qui pourrait faire rater l'expérience ?
S'il fait trop sombre ou que le mur que tu fixes à des dessins, tu ne verras pas bien. Choisi bien un mur de couleur unie.
Il faut bien regarder au delà de nos index.
Explications
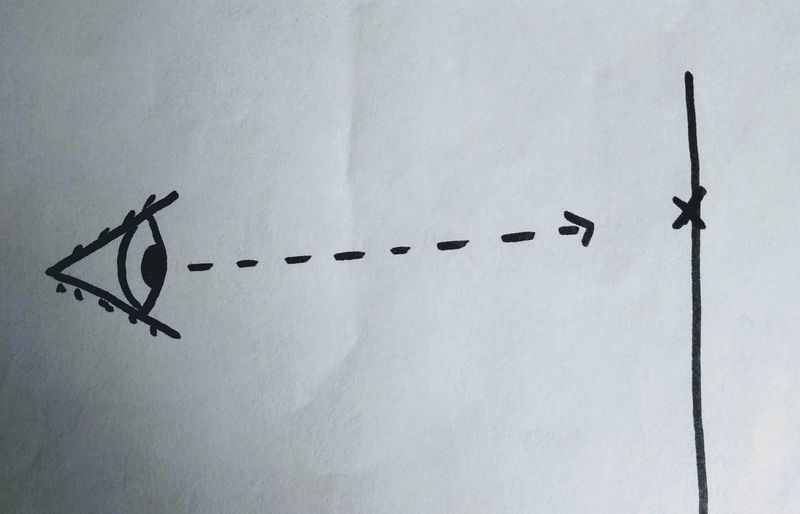
Comme le regard est fixé sur un point à l'horizon, lorsqu'un objet passe entre le regard et le point , il est déformé car l'oeil l'interprête mal.
Plus d'explications
L'illusion d'optique résulte d'une mauvaise interpretation du système visuel des informations qui lui parviennent. Le système visuel ne fonctionne pas comme un instrument de mesure, mais comme un moyen d'interagir efficacement avec l'environnement.
Dans l'expérience ordinaire, en cas de doute, un changement de point de vue donne une vision plus exacte de la réalité. Dans les illusions visuelles, cette possibilité est bloquée, entraînant une image faussée de la réalité, y compris faisant voir un objet inexistant, ou rendant « aveugle » à un objet pourtant présent.
https://fr.wikipedia.org/wiki/Illusion_d%27optique
Applications : dans la vie de tous les jours
On peut observer dans la rue des trompe-l'oeil qui créent l'illusion d'une profondeur sur une surface plane vue depuis un certain point. La peinture et le théâtre utilisent également cette technique pour donner des effets de profondeur et de volume.
Les illusionnistes et magiciens en font, aidés par des techniques de persuasion, une bonne part de leurs spectacles.
Éléments pédagogiques
Objectifs pédagogiques
Le but de cette expérience est d'introduire la notion d'illusion d'optique en montrant que l'on peut modifier notre perception des objets.
Sources et ressources
Illusion d'optique sur Wikipedia
Dernière modification 9/04/2020 par user:E.gohier.
Draft